Comment fonctionnent les antibiotiques ?
Tous les antibiotiques ont la propriété commune (Modes ou mécanismes d'action) d'interférer d'une certaine manière avec une fonction critique normale de la cellule bactérienne cible. Les antibiotiques les plus couramment utilisés exercent leur effet par l’une des méthodes suivantes :
- Inhibition de la synthèse de la paroi cellulaire (groupe I)
- Perturbation des membranes cellulaires (groupe II)
- Interférence avec la synthèse des protéines (groupe III)
- Interférence avec la synthèse d'acide nucléique (groupe IV)

Modes et mécanismes d'action des antibiotiques
Groupe I : Inhibiteurs de la synthèse de la paroi cellulaire
Les antibiotiques β-lactames, appelés ainsi parce qu’ils contiennent un noyau β-lactame dans leur structure, constituent le groupe principal qui fonctionne de la sorte. Les pénicillines et les céphalosporines font partie de ce groupe.
Vous vous souvenez peut-être de notre analyse de la structure de la paroi cellulaire bactérienne dans les articles précédents qu'un facteur important dans le renforcement du composant peptidoglycane des parois cellulaires bactériennes est la réticulation des chaînes par transpeptidation.
C’est ce processus sur lequel agissent les β-lactames; ils se lient de manière irréversible à l’enzyme transpeptidase en formant des liaisons covalentes avec un résidu sérine dans le site actif de l’enzyme. La paroi cellulaire continue à se former, mais s'affaiblit progressivement à mesure que de nouveaux peptidoglycanes non liés sont déposés. Étant donné que les bactéries se trouvent généralement dans un environnement hypotonique, lorsque la paroi s'affaiblit, de l'eau pénètre dans la cellule, ce qui entraîne un gonflement, puis une lyse.
Pénicillines: mode d'action
Le premier antibiotique β-lactame à avoir été découvert était la benzylpénicilline, ou pénicilline-G, dont l'action est limitée aux bactéries à Gram positif, car il est incapable de pénétrer dans la paroi cellulaire des Gram négatifs. Il est efficace contre les bactéries à Gram positif lorsqu’il est administré par voie intramusculaire, mais ne peut pas être pris par la bouche car il se décompose dans les conditions acides de l’estomac. Une autre pénicilline naturelle, la pénicilline-V, représente une avancée dans la mesure où elle est moins labile en acide et peut donc être prise par voie orale. Toutes les pénicillines sont basées sur une structure centrale ou un noyau appelé acide 6-amino-pénicillanique (Figure 14.2); des recherches approfondies ont abouti à la mise au point de nombreuses variantes de ce type de molécules, appelées pénicillines semi-synthétiques. Celles-ci se sont attachées à leur noyau de nouvelles chaînes latérales non rencontrées dans la nature et ont résolu certains des problèmes inhérents aux pénicillines naturelles telles que l’instabilité et la spécificité étroite (Figure 14.3).

- Les pénicillines semi-synthétiques sont basées sur la structure de base de la molécule naturelle, avec l’ajout de chaînes latérales synthétisées chimiquement.
Ampicillin: mode d'action
L'ampicilline est une pénicilline semi-synthétique qui a une spécificité plus large que la pénicilline G; il est nettement plus efficace contre les bactéries à Gram négatif telles que Salmonella et E. coli, sa nature hydrophobe le rendant plus apte à pénétrer dans leur membrane externe. Il présente l’avantage supplémentaire d’être stable en acide et peut donc être pris par voie orale.
Un autre inconvénient des pénicillines naturelles est qu'elles sont susceptibles aux β-lactamases bactériennes naturelles (également appelées pénicillinases), qui rompent une liaison dans le noyau β-lactame de la molécule de pénicilline (Figure 14.4). Parfois, les antibiotiques β-lactames sont pris en association avec un inhibiteur de β-lactamase tel que l’acide clavulanique. Ceci se lie à la β-lactamase avec une haute affinité l'empêchant d'agir sur l'antibiotique.
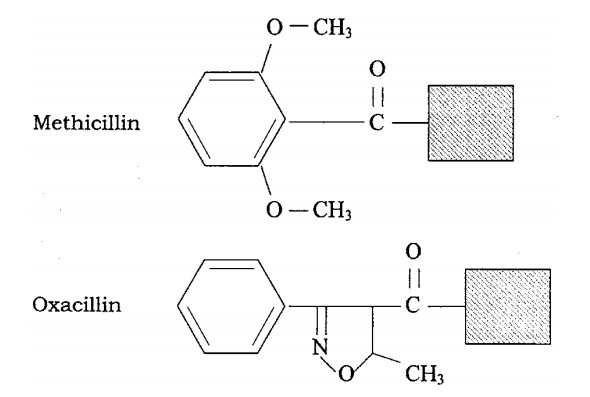
Certaines pénicillines semi-synthétiques telles que la méthicilline et l'oxacilline sont résistantes aux attaques des β-lactamases, qui peuvent rendre certaines bactéries résistantes à leurs formes naturelles.
La pénicilline n'est pas un traitement approprié pour environ 1 à 5% des adultes présentant une réaction allergique à cette substance; dans les cas extrêmes, le choc anaphylactique peut entraîner la mort.
Céphalosporines
Les céphalosporines, comme les pénicillines, ont une structure basée sur un cycle β-lactame (Figure 14.5). Ils exercent également leur effet sur les transpeptidases, mais ont généralement une spécificité plus large et sont plus résistants à l'action des β-lactamases.
La ceftriaxone, par exemple, est maintenant utilisée dans le traitement des infections à gonorrhée, causées par des souches de Neisseria gonorrhoeae résistantes à la pénicilline. De plus, les patients allergiques à la pénicilline sont souvent traités aux céphalosporines.
Céphalosporines : déouverte et application
Les céphalosporines ont été isolées pour la première fois à la fin des années 1940 dans un champignon marin appelé Cephalosporium acremonium et ont été généralisées dans les années 1960. Les céphalosporines de deuxième, troisième et quatrième générations ont été développées pour élargir le spectre d'activité à de nombreux organismes à Gram négatif et pour garder une longueur d'avance sur les agents pathogènes développant une résistance aux versions antérieures. Les pénicillines et les céphalosporines sont également utilisées à titre prophylactique, c'est-à-dire dans la prévention des infections, avant l'intervention chirurgicale chez les patients particulièrement vulnérables.

- Les antibiotiques β-lactames ont un deuxième mode d'action. Les β-lactames agissent également en empêchant la régulation naturelle des enzymes appelées autolysines. Ces enzymes agissent en décomposant le peptidoglycane de manière contrôlée, provoquant des ruptures permettant l'ajout d'un nouveau peptidoglycane à mesure que la cellule se développe, et sont normalement régulées par des inhibiteurs naturels. Les β-lactamines neutralisent l'activité de ces inhibiteurs, entraînant une dégradation supplémentaire de la paroi cellulaire.
Autres antibiotiques qui affectent la paroi cellulaire
Carbapénèmes
Les carbapénèmes sont des antibiotiques β-lactames produits naturellement par une espèce de Streptomyces. Une forme semi-synthétique, imipenem, est active contre un large éventail de bactéries à Gram positif et négatif et est utilisée lorsque la résistance aux autres β-lactames s'est développée.
Bacitracine
La bacitracine et la vancomycine sont deux autres antibiotiques qui exercent leur effet sur la paroi cellulaire mais par un mécanisme différent. La bacitracine est dérivée de l'espèce de Bacillus et agit sur le pyrophosphate de bactoprenol, la molécule porteuse des lipides responsable du transport des unités de peptidoglycane à travers la membrane cellulaire jusqu'à leur site d'incorporation dans la paroi cellulaire.
Son utilisation est limitée à l'application topique (surface) car son utilisation en interne peut provoquer des lésions rénales. La vancomycine est un antibiotique hautement toxique dont le spectre d'utilisation est limité contre les organismes à Gram positif, tels que les streptocoques et les staphylocoques. Il est particulièrement important dans son utilisation contre les infections causées par des organismes résistants à la méthicilline et aux céphalosporines, tels que Staphylococcus aureus résistant à la méthicilline (SARM). Il n'est pas absorbé par le tractus gastro-intestinal et est donc administré le plus souvent par voie intraveineuse.
- Large spectre ou spectre étroit?
Certains antibiotiques, en raison du mécanisme de leur action, ne sont efficaces que contre quelques agents pathogènes différents, alors que d'autres peuvent être utilisés avec succès contre de nombreux types différents. On dit qu'ils ont respectivement un spectre étroit et un large spectre d'activité.
À première vue, toutes choses étant égales par ailleurs, vous vous attendez à ce que votre médecin choisisse l’antibiotique ayant le spectre d’activités le plus large possible, mais ce n’est pas toujours l’option la plus sage. Lorsque la cause d’une infection n’est pas connue, il est judicieux de se protéger et de prescrire un antibiotique à large spectre («quoi que ce soit, ça devrait trier!»), Mais cette politique n’est pas sans danger. Le médicament est susceptible de tuer beaucoup de la microflore résidante de l’hôte, ce qui peut conduire à une surinfection, et le développement de souches résistantes aux antibiotiques est également rendu plus probable. Si l'identité de l'agent pathogène est suspectée, un médicament à spectre étroit approprié doit être préféré.

0 Commentaires